「MD安德森癌症中心」最新综述解读:全球核药发展现状
2025年2月1日,MD安德森癌症中心发表在《European Journal of Nuclear Medicine and Molecular Imaging》上的一篇题为“Radiotheranostic landscape: A review of clinical and preclinical development”的综述文章,全面评估了放射性治疗诊断领域的最新进展。该文章由Ha H. Tran、Aiko Yamaguchi和H. Charles Manning撰写,深入探讨了放射性治疗诊断在临床和临床前研究中的发展现状、新兴趋势以及面临的挑战,揭示了放射性诊疗在肿瘤治疗中的巨大潜力。
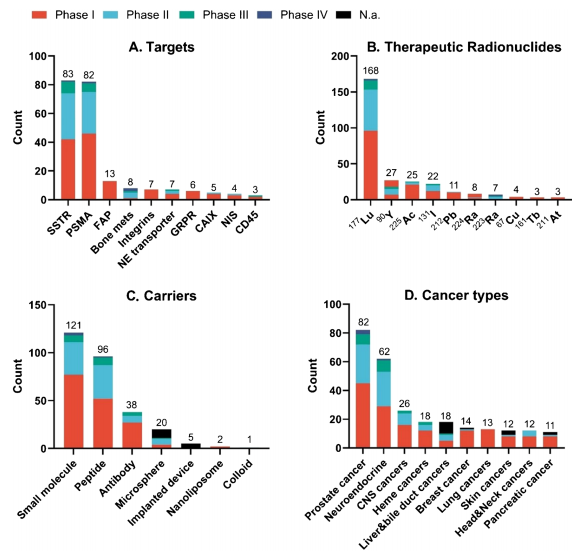

图片来源:文献原文
靶点创新:从成熟靶标到泛癌突破
SSTR和PSMA:现有药物如Lutathera®和Pluvicto®在神经内分泌肿瘤和前列腺癌中的应用已获得批准,且正在探索其在前线治疗中的应用。177Lu标记的DOTATATE已拓展至脑膜瘤临床试验,而PSMA靶向疗法Pluvicto®在早期前列腺癌中的III期数据即将公布。
新型靶点:FAP、CAIX(碳酸酐酶IX)、GRPR、CD标记物和整合素等新型靶点正在临床试验中接受评估,显示出在多种肿瘤类型中的潜力。其中成纤维细胞活化蛋白(FAP)抑制剂表现亮眼,177Lu-FAPI在胰腺癌Ⅰ期试验中达到62%的疾病控制率;整合素αvβ3/β6靶向探针则突破实体瘤异质性难题,在肺癌肝转移灶中显示特异性蓄积。
核素革命:α粒子疗法破局微小病灶
锕-225(²²⁵Ac)因其高线性能量转移(LET)特性,成为攻克微转移的"核武器"。2024年欧洲核医学年会披露,²²⁵Ac-PSMA治疗去势抵抗性前列腺癌患者的中位生存期达18.7个月,较传统治疗提升41%。而铽-161(¹⁶¹Tb)通过释放β⁻与俄歇电子的双重杀伤机制,在卵巢癌腹膜转移模型中实现肿瘤体积缩小92%。核素供应链瓶颈也在突破,美国启动首个²²⁵Ac规模化生产设施,预计2026年产能提升300%。
载体工程:智能递送系统降毒增效
在载体方面,双特异性抗体与纳米载体技术成为研究热点。CD38/CD47双抗搭载²¹²Pb,在多发性骨髓瘤治疗中骨髓毒性降低70%;可降解硅基纳米颗粒携载¹⁷⁷Lu,在肝癌模型显示肿瘤/肝摄取比达15:1。预靶向技术通过"点击化学"分步递送,使α核素治疗剂量提升3倍而不增加正常组织损伤。
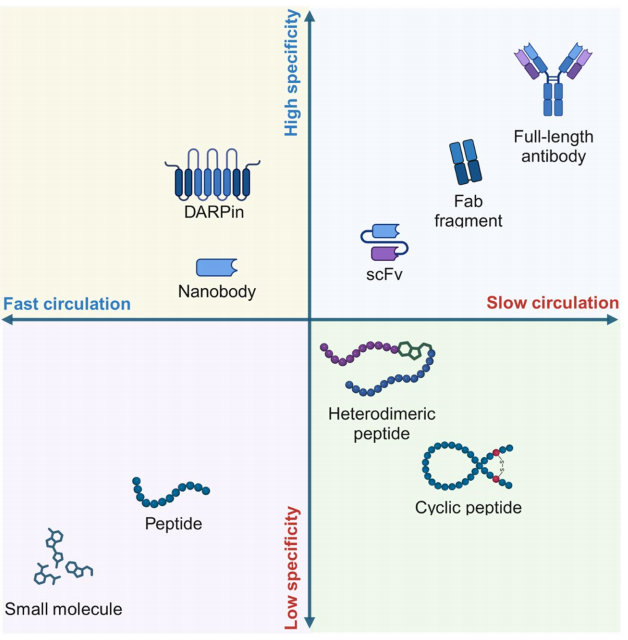
不同的放射性核素载体的优缺点
图片来源:文献原文
关键挑战与未来方向
尽管前景广阔,核素全球供应缺口仍制约发展。目前²²⁵Ac年产量不足100居里,难以满足临床需求。监管层面,EMA正推动建立α核素治疗国际标准。值得期待的是,放射性免疫联合疗法(如PSMA-PD1联用)在Ⅱ期试验中客观缓解率提升至58%,或将成为下一个爆发点。随着人工智能驱动的剂量优化系统进入临床,放射治疗诊断学正朝着"全癌种覆盖、全周期管理"的目标加速迈进。
注:原创
原文链接:https://link.springer.com/article/10.1007/s00259-025-07103-7


